Cos'è l'anodo e il catodo - una semplice spiegazione
Elettrochimica e galvanica
Ci sono due sezioni principali in elettrochimica:
- Celle galvaniche - la produzione di elettricità attraverso una reazione chimica. Questi elementi includono batterie e accumulatori. Sono spesso chiamate fonti di corrente chimica.
- L'elettrolisi - l'impatto su una reazione chimica con l'elettricità, in parole semplici - con l'aiuto di una fonte di energia, inizia una reazione.
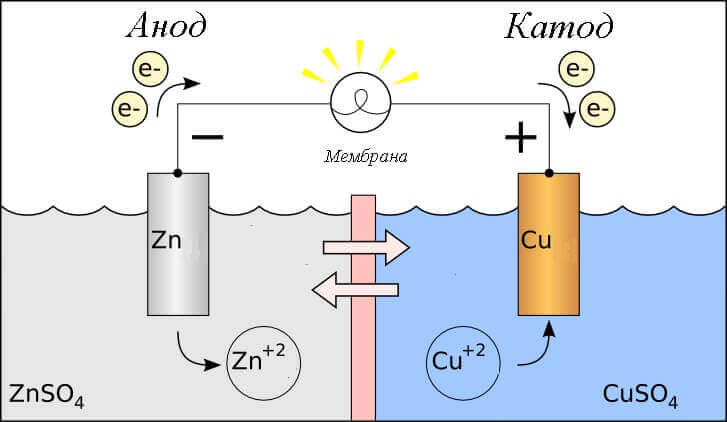
Considera la reazione redox in una cella galvanica, quindi quali processi avvengono sui suoi elettrodi?
- anodo - l'elettrodo su cui si osserva reazione ossidativacioè luidà elettroni. Viene chiamato l'elettrodo su cui si verifica la reazione di ossidazione agente riducente.
- catodico - l'elettrodo sul quale scorre reazione di recuperocioè luiaccetta elettroni. Viene chiamato l'elettrodo su cui si verifica la reazione di riduzione agente ossidante.
Questo pone la domanda: dov'è il plus e dov'è il meno della batteria? Basato sulla definizione di una cella galvanica l'anodo dà elettroni.
! importante GOST 15596-82 fornisce una definizione ufficiale dei nomi delle conclusioni delle fonti di corrente chimica, in breve, quindi più al catodo e meno all'anodo.
In questo caso, viene considerato il flusso di corrente elettrica. lungo il conduttore del circuito esterno da ossidante (catodo) a riducente (Anodo). Poiché gli elettroni nel circuito scorrono da meno a più e la corrente elettrica è viceversa, allora il catodo è un plus e l'anodo è un meno.
Attenzione: la corrente scorre sempre nell'anodo!
O lo stesso nel diagramma:
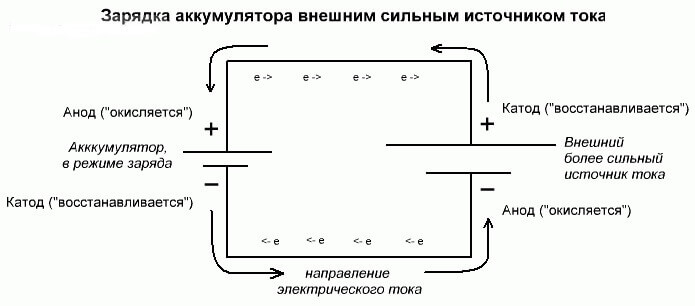
Elettrolisi della batteria o processo di ricarica
Questi processi sono simili e inversi rispetto alla cella galvanica, poiché qui l'energia non proviene da una reazione chimica, ma piuttosto una reazione chimica si verifica da una fonte esterna di elettricità.
In questo caso, oltre all'alimentazione viene anche chiamato catodo e meno l'anodo. Ma i contatti della cella galvanica ricaricabile o degli elettrodi dell'elettrolizzatore avranno già nomi opposti, vediamo perché!
! importante Quando una cella galvanica viene scaricata, l'anodo è meno, il catodo è più e viceversa durante la carica.
Poiché la corrente proveniente dal terminale positivo della fonte di alimentazione viene fornita al terminale positivo della batteria, quest'ultimo non può più essere un catodo.Facendo riferimento a quanto sopra, possiamo concludere che in questo caso gli elettrodi della batteria cambiano condizionatamente i luoghi durante la ricarica.
Quindi, attraverso l'elettrodo di una cella galvanica carica in cui scorre una corrente elettrica, viene chiamato un anodo. Si scopre che quando si carica la batteria, il più diventa l'anodo e il meno il catodo.
galvanotecnica
I processi di deposizione di metallo a seguito di una reazione chimica sotto l'influenza di una corrente elettrica (durante l'elettrolisi) sono chiamati ingegneria galvanica. Pertanto, il mondo ha ricevuto gioielli e dettagli placcati in argento, dorati, cromati o altri metalli. Questo processo viene utilizzato sia per scopi decorativi che per scopi applicati - per migliorare la resistenza alla corrosione di vari componenti e gruppi di meccanismi.
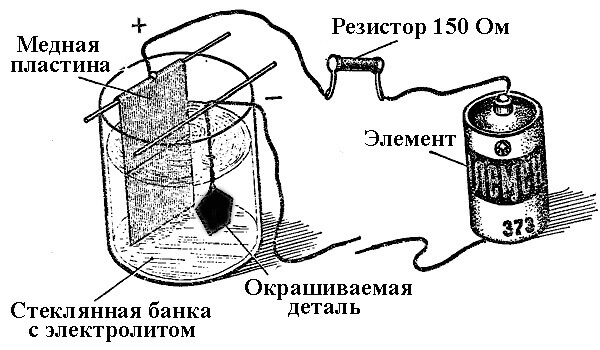
Il principio di funzionamento degli impianti di galvanizzazione risiede nell'uso di soluzioni di sali degli elementi che copriranno la parte come elettrolita.
Nella galvanica, l'anodo è anche un elettrodo a cui è collegata l'uscita positiva della fonte di alimentazione, rispettivamente, il catodo in questo caso è un meno. In questo caso, il metallo viene depositato (ridotto) sull'elettrodo negativo (reazione di riduzione). Cioè, se si desidera creare un anello dorato con le proprie mani, collegare l'uscita negativa dell'alimentatore ad esso e metterlo in un contenitore con la soluzione appropriata.
In elettronica
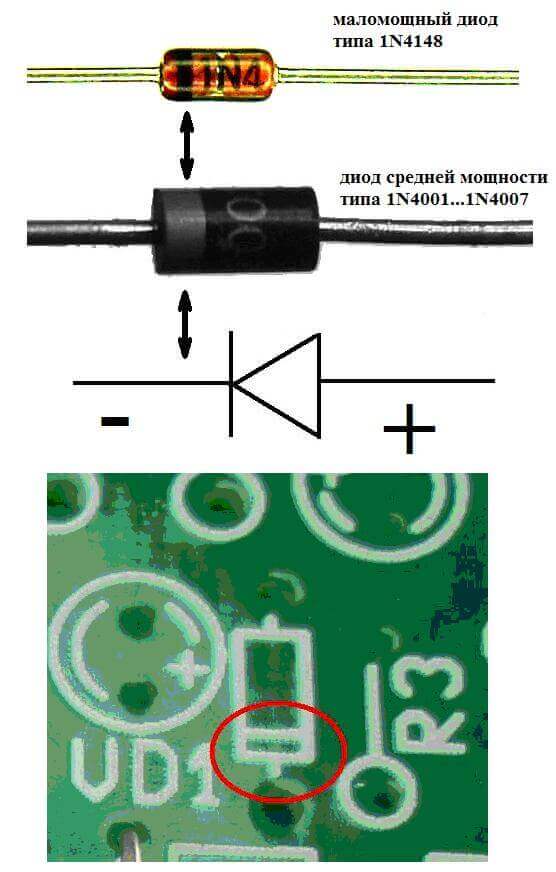
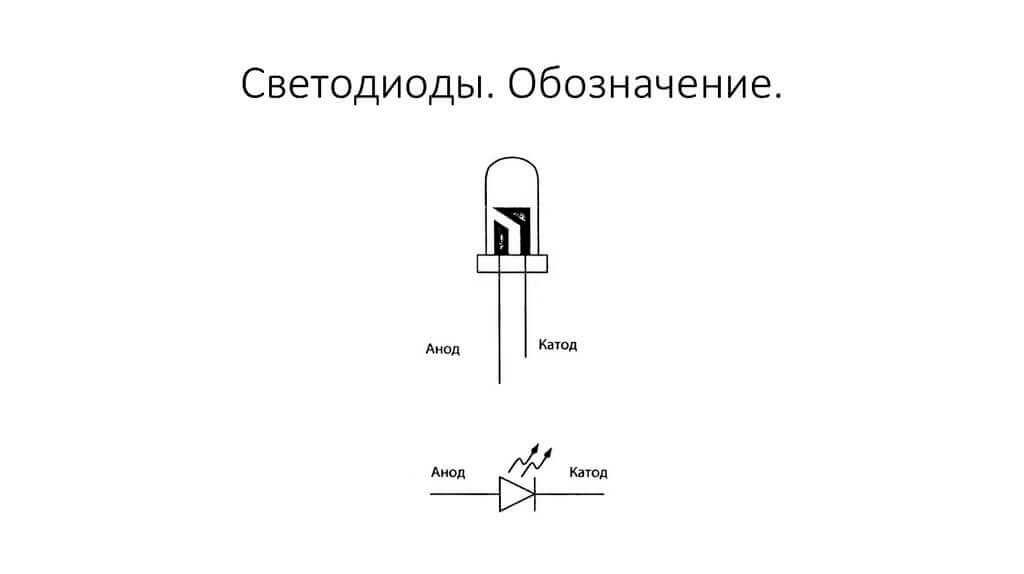
Gli elettrodi o le gambe dei dispositivi elettronici a semiconduttore e sotto vuoto sono spesso chiamati anodo e catodo. Considera la designazione grafica condizionale di un diodo a semiconduttore nel diagramma:
Come vediamo, l'anodo del diodo è collegato al plus della batteria. È così chiamato per lo stesso motivo: in questo caso, la corrente scorre nell'uscita del diodo in ogni caso. Su un elemento reale sul catodo è presente una marcatura sotto forma di una striscia o un punto.
Il LED è simile. Sui LED da 5 mm, gli interni sono visibili attraverso il pallone. La metà più grande è il catodo.
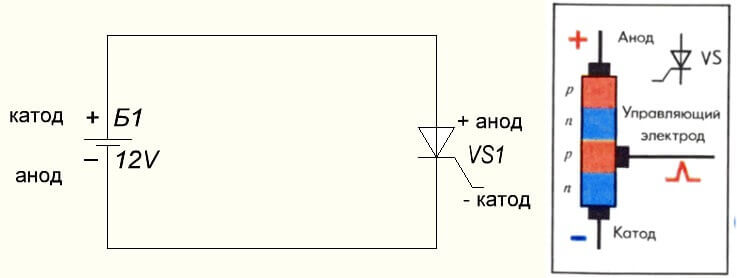
La situazione è anche con il tiristore, lo scopo delle conclusioni e l'applicazione "unipolare" di questi componenti a tre gambe lo rendono un diodo controllato:
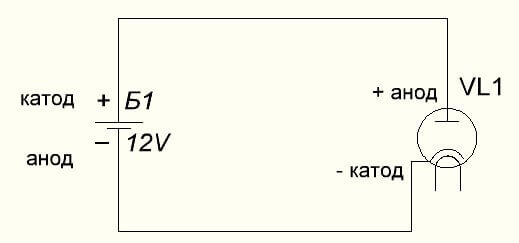
Il diodo del vuoto collega anche l'anodo al più e il catodo al meno, che è mostrato nello schema seguente. Sebbene quando si applica la tensione inversa, i nomi di questi elementi non cambieranno, nonostante il flusso di corrente elettrica nella direzione opposta, sebbene insignificante.
Con elementi passivi come condensatori e resistori, non è così. Il catodo e l'anodo non sono isolati separatamente dalla resistenza; la corrente al suo interno può fluire in qualsiasi direzione. Puoi dare qualsiasi nome alle sue conclusioni, a seconda della situazione e dello schema in questione. Condensatori non polari convenzionali anche. Meno comunemente, questa separazione dei nomi dei contatti viene osservata nei condensatori elettrolitici.
conclusione
Quindi, per riassumere, rispondendo alla domanda: come ricordare dov'è il plus, dov'è il meno del catodo con l'anodo? Esiste una pratica regola mnemonica per i dispositivi di elettrolisi, carica della batteria, galvanica e semiconduttori. Queste parole con nomi simili hanno lo stesso numero di lettere, come illustrato di seguito:
In tutti questi casi, la corrente fluisce dal catodo e fluisce nell'anodo.
Non essere confuso dalla confusione: "perché il catodo è positivo per la batteria e quando viene caricato diventa negativo?" Ricorda per tutti gli elementi dell'elettronica, oltre che per gli elettrolizzatori e la galvanica - in generale, per tutti i consumatori di energia, l'anodo è l'uscita collegata al plus. Le differenze finiscono qui, ora è più facile per te capire qual è il vantaggio e il meno tra le uscite degli elementi e dei dispositivi.
Infine, ti consigliamo di guardare un utile video sull'argomento dell'articolo:
Ora sai cosa sono l'anodo e il catodo e come ricordarli abbastanza rapidamente. Speriamo che le informazioni fornite siano state utili e interessanti per te!
Materiali correlati: